circNDUFB2通過使IGF2BP不穩(wěn)定并激活抗腫瘤免疫力來抑制非小細胞肺癌的進展
肺癌是最常被診斷的癌癥之一,也是導(dǎo)致癌癥死亡的主要原因,非小細胞肺癌(NSCLC)約占肺癌病例的85%。環(huán)狀RNA(circRNA)是一類共價閉合的單鏈RNA,與癌癥的發(fā)展有關(guān)。今天我們來看一篇發(fā)表在Nature Communications期刊的一篇文章,題名為:circNDUFB2 inhibits non-small cell lung cancer progression via destabilizing IGF2BPs and activating anti-tumor immunity。
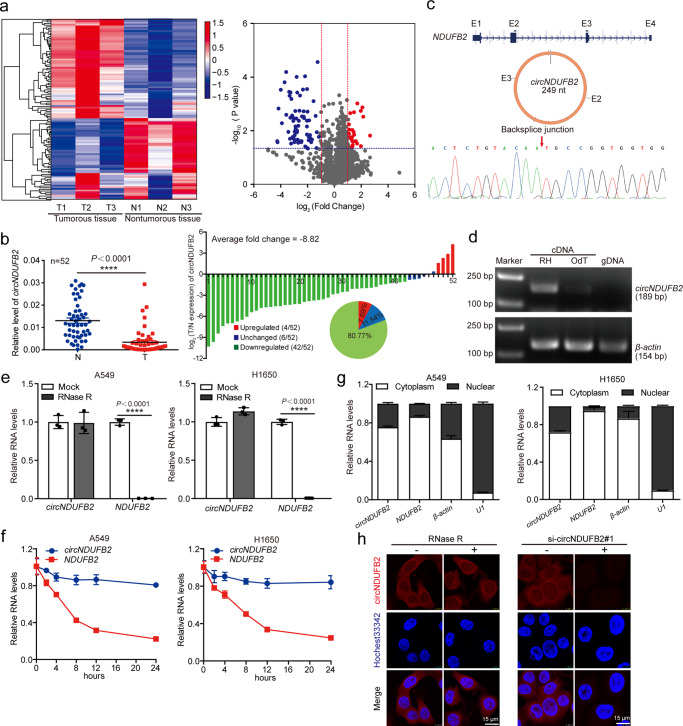
circNDUFB2在NSCLC中被下調(diào)
通過circRNA芯片分析了三對NSCLC樣品中circRNA的表達譜,總共鑒定出109個circRNA失調(diào),33個上調(diào),76個下調(diào)。qRT-PCR驗證52個配對NSCLC樣品中前五差異circRNA的表達。circNDUFB2是最顯著下調(diào)的circRNA。臨床分析發(fā)現(xiàn)circNDUFB2高表達與NSCLC患者的腫瘤大小、淋巴結(jié)轉(zhuǎn)移和分期呈負相關(guān)。結(jié)果表明,circNDUFB2在NSCLC中經(jīng)常被下調(diào),并且與NSCLC的惡性特征呈負相關(guān)。circNDUFB2由NDUFB2基因的外顯子2–3產(chǎn)生,長度為249 nt。circNDUFB2可由發(fā)散引物擴增,收斂引物不能擴增。核酸酶消化證實circNDUFB2具有閉環(huán)結(jié)構(gòu)。放線菌素D處理表明,與NDUFB2 mRNA相比,circNDUFB2是穩(wěn)定的。核質(zhì)分離PCR以及熒光原位雜交(FISH)顯示circNDUFB2主要定位于細胞質(zhì)中。這些結(jié)果表明circNDUFB2是一個circRNA。
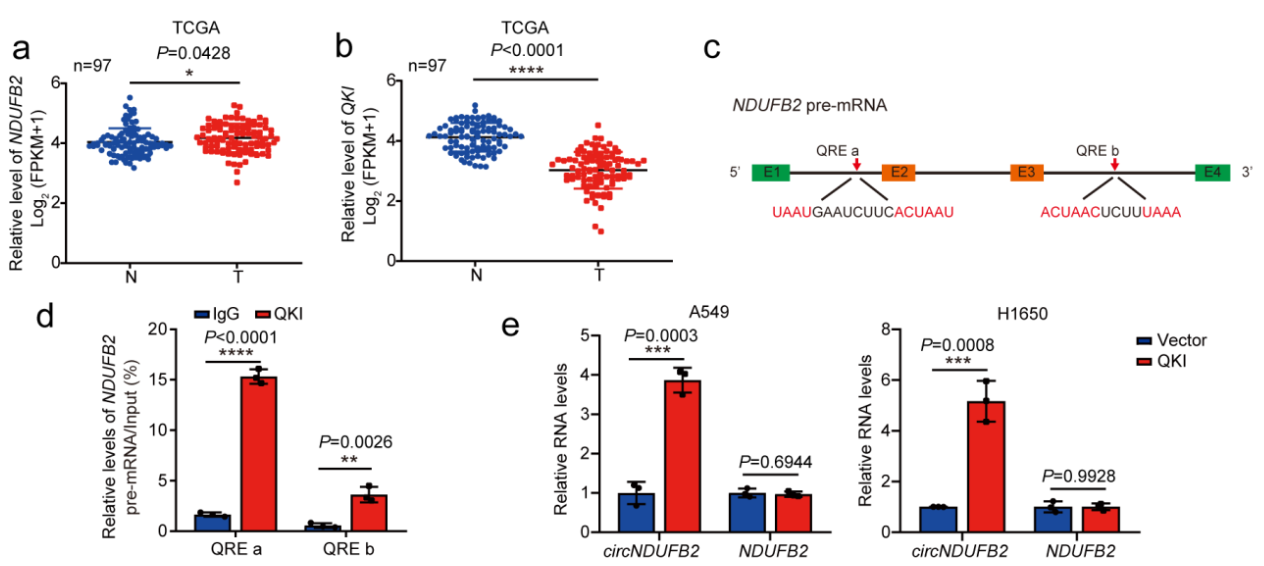
QKI促進NSCLC細胞中circNDUFB2的生物發(fā)生
circNDUFB2和NDUFB2均來自NDUFB2 pre-mRNA,而NDUFB2 mRNA在NSCLC中略有上調(diào)。因此,推測circNDUFB2的下調(diào)在轉(zhuǎn)錄后發(fā)生。我們在circNDUFB2中搜索與潛在QRE匹配的序列。接下來進行了RIP分析,確認QKI確實與NDUFB2 pre-mRNA中的假定QRE結(jié)合。在NSCLC細胞中QKI過表達可能會上調(diào)circNDUFB2。 這些數(shù)據(jù)表明,QKI與NDUFB2 pre-mRNA的circNDUFB2形成外顯子側(cè)翼的內(nèi)含子結(jié)合,從而促進circNDUFB2的形成。
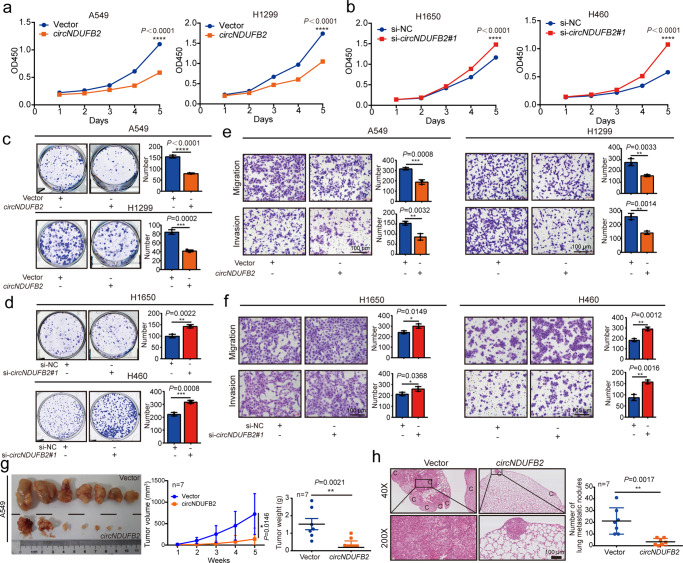
circNDUFB2抑制NSCLC進展
體外研究表明circNDUFB2過表達顯著抑制了NSCLC細胞的增殖,遷移和侵襲,而circNDUFB2敲低顯著促進了這些表型。體內(nèi)實驗表明circNDUFB2過表達可顯著抑制NSCLC細胞的致瘤性和轉(zhuǎn)移。這些數(shù)據(jù)表明circNDUFB2可能在NSCLC進展中起抑制作用。
circNDUFB2與NSCLC細胞中的IGF2BP1/2/3相互作用
為了探索circNDUFB2是否通過與蛋白質(zhì)相互作用發(fā)揮功能,RNA pulldown來鑒定與其相關(guān)的蛋白質(zhì)。RNApulldown沉淀物通過SDS-PAGE分離。銀染后,切下約65 kDa的有義特異性條帶,并使用質(zhì)譜進行分析。發(fā)現(xiàn)前三個豐富的蛋白質(zhì)分別是IGF2BP2,IGF2BP1和IGF2BP3。使用Western blot和RIP分析證實了這一結(jié)果。此外, RNA FISH免疫熒光分析,發(fā)現(xiàn)circNDUFB2與IGF2BPs共定位在細胞質(zhì)中。為了探討IGF2BPs的KH域?qū)τ谂ccircNDUFB2之間的相互作用,構(gòu)建IGF2BPs突變體,KH結(jié)構(gòu)域突變明顯減少了IGF2BP與circNDUFB2之間的相互作用。接下來進行了circNDUFB2突變,發(fā)現(xiàn)circNDUFB2突變顯著降低了IGF2BP與circNDUFB2之間的相互作用。
IGF2BP結(jié)合區(qū)域包含“ GGAC” N6-甲基腺苷(m6A)核心基序。IGF2BPs是m6A結(jié)合蛋白。為了探索circRNA和IGF2BP之間的相互作用是否通過m6A依賴性的方式進行調(diào)節(jié),對circNDUFB2進行了MeRIP,并觀察到circNDUFB2中m6A的顯著富集。敲低METTL3和METTL14顯著降低了circNDUFB2中m6A修飾的水平,并且沒有改變circNDUFB2的水平。METTL3 / 14敲低顯著削弱了circNDUFB2和IGF2BP之間的相互作用。 這些數(shù)據(jù)表明,circNDUFB2以依賴于m6A的方式與三個IGF2BP物理相互作用。
circNDUFB2過表后IGF2BPs的mRNA無顯著變化,蛋白質(zhì)水平顯著降低。此外,circNDUFB2突變體不影響IGF2BPs的蛋白質(zhì)水平。因此推測circNDUFB2可能通過相互作用使IGF2BP蛋白失穩(wěn)。發(fā)現(xiàn)circNDUFB2的過度表達顯著降低了IGF2BP蛋白的水平,這可以通過MG132(蛋白酶抑制劑)恢復(fù)。circNDUFB2顯著增加了IGF2BPs的泛素化水平,但這種作用因其突變而受損。這些結(jié)果表明circNDUFB2通過促進泛素/蛋白酶體依賴性降解降低IGF2BPs的穩(wěn)定性。
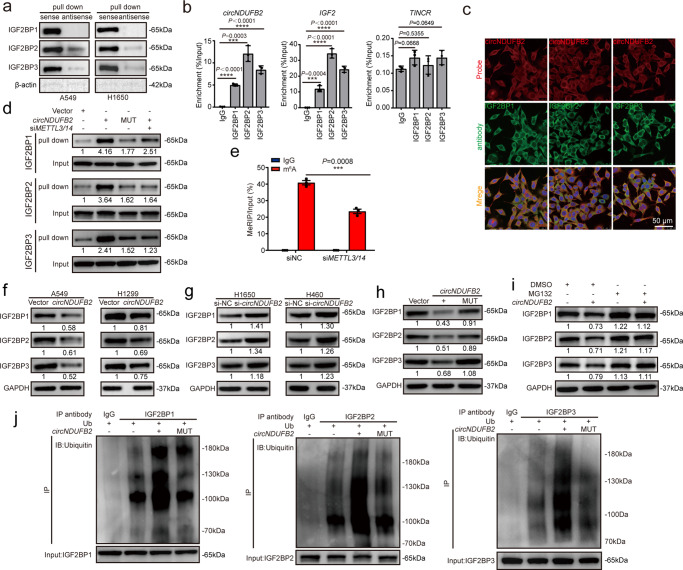
TRIM25是介導(dǎo)IGF2BP泛素化的E3連接酶
為了進一步鑒定IGF2BPs泛素化的E3連接酶,RNA pulldown質(zhì)譜結(jié)果中在156種潛在的相互作用蛋白中發(fā)現(xiàn)了兩種E3連接酶TRIM25和HECTD3。 使用WB分析, TRIM25與circNDUFB2特異性相關(guān)。 RIP分析進一步證實了circNDUFB2與TRIM25的關(guān)聯(lián)。RNA FISH免疫熒光分析表明circNDUFB2與TRIM25在細胞質(zhì)中共定位。進行Co-IP結(jié)果顯示TRIM25與所有三個IGF2BP結(jié)合。免疫熒光分析表明TRIM25與所有三個IGF2BP蛋白共定位在細胞質(zhì)中。IGF2BPs的mRNA水平不受TRIM25的影響,但是在TRIM25敲低時,IGF2BPs的蛋白水平顯著增加,而在TRIM25的過表達中,IGF2BPs的蛋白水平分別降低。在TRIM25過表達的A549細胞中,IGF2BP的泛素化水平顯著增加。這些結(jié)果表明,TRIM25是E3泛素連接酶,可與IGF2BP蛋白相互作用,并通過泛素-蛋白酶體途徑降解NSCLC細胞。
TRIM25的RNA結(jié)合活性對于其對底物的泛素連接酶活性是必需的。構(gòu)建了一個帶有FLAG標記RNA結(jié)合域(RBD)缺失突變體。TRIM25ΔRBD不影響IGF2BPs的蛋白質(zhì)水平,對IGF2BPs的泛素化水平?jīng)]有明顯影響,表明TRIM25完整的RBD對于IGF2BPs的有效泛素化和降解是必要的。這些結(jié)果表明,TRIM25通過泛素-蛋白酶體途徑促進NSCLC細胞中IGF2BPs的降解,并且TRIM25的RNA結(jié)合活性對其在底物泛素化中的作用至關(guān)重要。

已經(jīng)顯示,TRIM25使用RNA作為其靶標有效泛素化的支架。然后,探討了TRIM25對IGF2BPs的泛素連接酶活性是否取決于circNDUFB2的存在。 circNDUFB2的丟失顯示了TRIM25對IGF2BPs泛素化和降解的顯著減弱作用。進一步驗證實驗數(shù)據(jù)并檢查circNDUFB2是否充當(dāng)支架來增強TRIM25與IGF2BP的結(jié)合,進行了Co-IP分析。在帶有circNDUFB2但沒有circNDUFB2-MUT過表達的A549細胞中,TRIM25和IGF2BP之間的關(guān)聯(lián)得到增強。由于circNDUFB2對RNA核酸外切酶的抗性,使用RNase A治療會嚴重破壞相互作用。此外,在METTL3 / 14敲低后,IGF2BP的泛素化作用顯著降低。結(jié)果表明,circNDUFB2充當(dāng)支架,以增強TRIM25和IGF2BPs之間的相互作用,隨后促進TRIM25介導(dǎo)的IGF2BPs泛素化和降解。
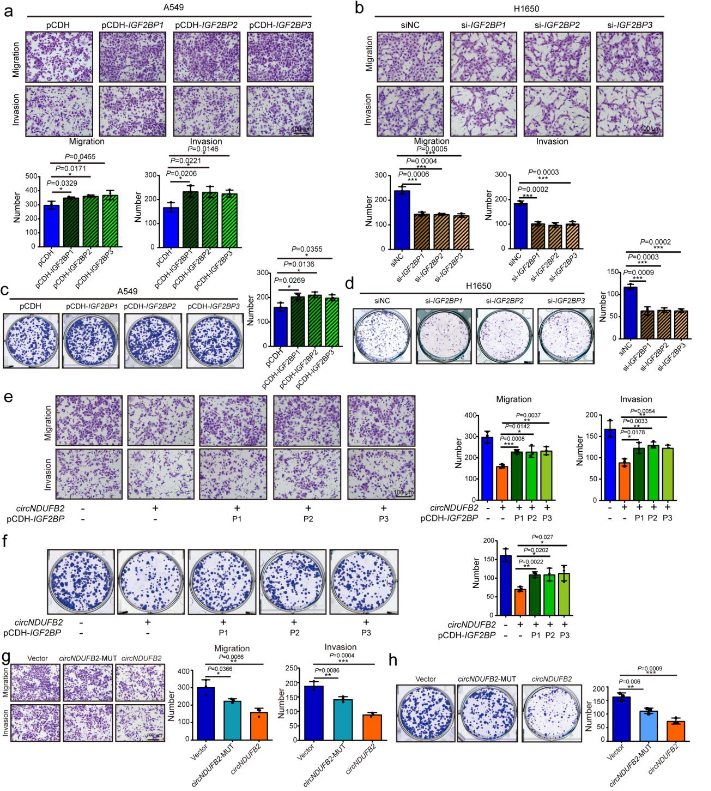
IGF2BPs是circNDUFB2的下游功能性蛋白
IGF2BPs是致癌蛋白,circNDUFB2可降低IGF2BPs的穩(wěn)定性,推測IGF2BPs介導(dǎo)circNDUFB2對NSCLC進展的影響。IGF2BPs過表達顯著增加了A549細胞的遷移和侵襲能力以及集落形成能力。IGF2BPs敲除顯著降低H1650細胞的遷移和侵襲能力以及集落形成能力。這些結(jié)果證實IGF2BPs是NSCLC的促瘤因子。隨后,觀察到IGF2BPs過度表達僅部分恢復(fù)了circNDUFB2過度表達減少的遷移和侵襲能力以及集落形成能力,表明circNDUFB2部分通過降解IGF2BPs發(fā)揮腫瘤抑制作用。盡管circNDUFB2 MUT不影響IGF2BPs的蛋白質(zhì)水平但它仍然對NSCLC細胞的進展具有抑制作用。這些數(shù)據(jù)表明circNDUFB2 MUT的抑制作用除了降解IGF2BPs外,還可能與circNDUFB2的其他機制有關(guān)。
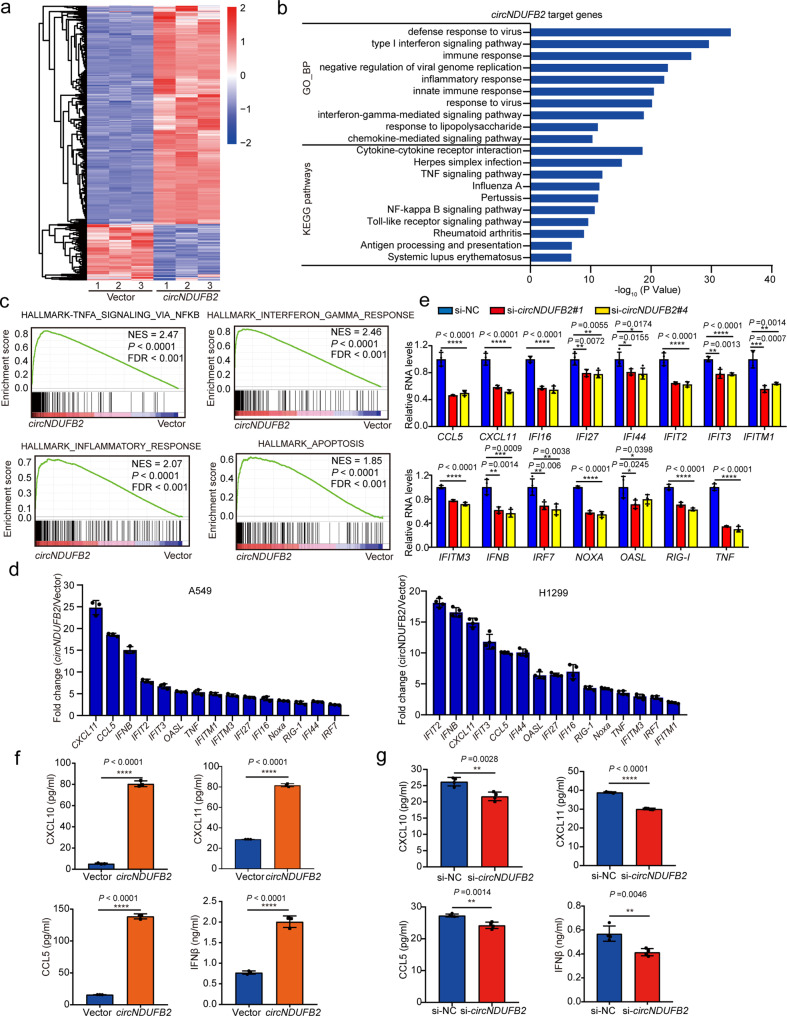
circNDUFB2觸發(fā)NSCLC細胞的免疫防御反應(yīng)
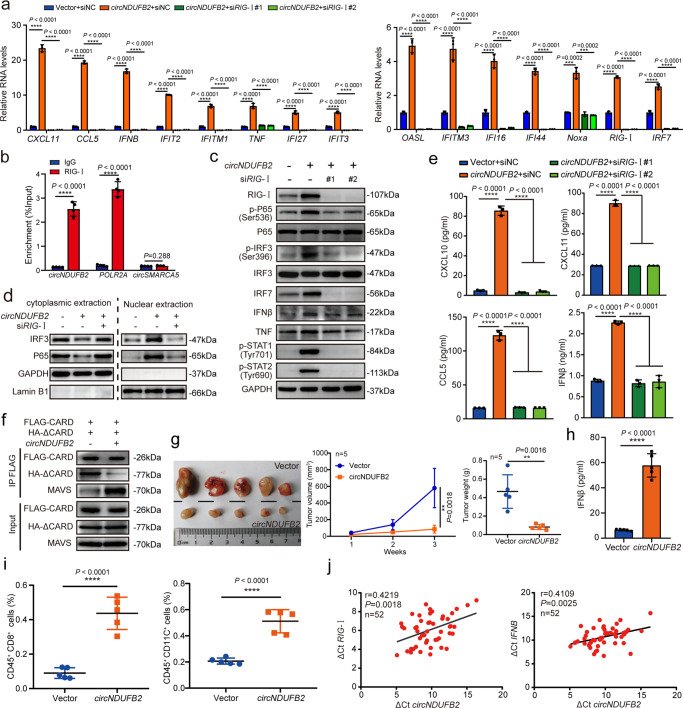
為了研究參與circNDUFB2的信號通路,使用RNA測序(RNA-seq)進行了轉(zhuǎn)錄組分析。結(jié)果表明circNDUFB2過表達影響934個基因的表達水平,其中743個基因上調(diào),191個基因被下調(diào)。基因本體生物學(xué)過程(GO_BP)和KEGG途徑富集分析表明circNDUFB2觸發(fā)了免疫防御和I型干擾素(IFNs)信號傳導(dǎo)。基因集富集分析(GSEA)也表明目標基因的信號傳導(dǎo)途徑參與了免疫反應(yīng)。確認了在circNDUFB2過表達的NSCLC細胞中一組免疫基因表達被上調(diào),而circNDUFB2敲低降低了NSCLC細胞中這些基因的水平。這些結(jié)果表明,過量表達circNDUFB2,而不是其具有相同序列的線性RNA片段,導(dǎo)致免疫基因上調(diào)。 酶聯(lián)免疫吸附試驗(ELISA)證實circNDUFB2過表達顯著增加了細胞培養(yǎng)上清液中CXCL10,CXCL11,CCL5和IFNβ的水平,而circNDUFB2敲低降低了細胞培養(yǎng)上清液中這些細胞因子的水平。這些結(jié)果證明circNDUFB2在NSCLC細胞中引發(fā)免疫應(yīng)答。
RIG-I對circNDUFB2誘導(dǎo)的免疫反應(yīng)至關(guān)重要
RIG-I樣受體(RLR)家族可識別病毒RNA 會通過產(chǎn)生IFN和促炎性細胞因子來觸發(fā)針對病毒感染的先天免疫反應(yīng)。已經(jīng)報道外源circRNA有效刺激由RIG-1介導(dǎo)的免疫信號傳導(dǎo)。從qRT-PCR分析獲得的數(shù)據(jù)表明,RIG-1敲低消除了circNDUFB2過表達誘導(dǎo)的免疫反應(yīng),RIG-1被circNDUFB2上調(diào)。為了研究circNDUFB2和RIG-I之間的關(guān)聯(lián),進行RIP分析和RNA FISH免疫熒光實驗。 結(jié)果表明circNDUFB2與RIG-1結(jié)合,并且它們共定位在細胞質(zhì)中。 circNDUFB2過表達后, circNDUFB2顯著上調(diào)了RIG-1,IRF7,IFNβ和TNF的蛋白水平,而circNDUFB2則不影響P65和IRF3的蛋白水平。同時,circNDUFB2顯著增加了p-P65,p-IRF3,p-STAT1和p-STAT2。circNDUFB2還促進了IRF3和P65進入核內(nèi)的易位。免疫熒光分析證實circNDUFB2促進了IRF3的磷酸化,并隨后觸發(fā)其轉(zhuǎn)移到細胞核中。更重要的是,RIG-1的敲除顯著消除了這些基因的蛋白質(zhì)水平或磷酸化水平的上調(diào)以及由circNDUFB2誘導(dǎo)的A549細胞中IRF3和P65的核易位。ELISAs測量細胞培養(yǎng)上清液中的細胞因子水平,發(fā)現(xiàn)RIG-1敲低顯著消除了對CXCL10,CXCL11,CCL5和IFNβ的誘導(dǎo)。上述結(jié)果表明RIG-1在介導(dǎo)NSCLC細胞中circNDUFB2的免疫應(yīng)答中起關(guān)鍵作用,而circNDUFB2引發(fā)的免疫應(yīng)答不依賴于circNDUFB2中m6A的修飾。
在沒有RNA配體的情況下,RIG-I采用一種自動抑制的構(gòu)象,CARDs發(fā)出信號。因此假設(shè)circNDUFB2可能通過促進其CARDs釋放激活RIG-I。用Co-IP檢測RIG-I的CARDs(FLAG-CARD)和螺旋酶結(jié)構(gòu)域(HA-ΔCARD)之間的相互作用。結(jié)果表明circNDUFB2抑制了RIG-I的CARDs和螺旋酶結(jié)構(gòu)域之間的相互作用。此外,circNDUFB2增強了CARDs與線粒體抗病毒信號蛋白(MAVS)的相互作用。這些結(jié)果表明circNDUFB2可能通過破壞CARDs與其解旋酶結(jié)構(gòu)域之間的分子內(nèi)相互作用來激活RIG-I,并使RIG-I保持活性,從而激活RIG-I-MAVS信號級聯(lián)。
circNDUFB2的免疫反應(yīng)抑制NSCLC進展
為了研究circNDUFB2是否具有刺激免疫反應(yīng)的潛力,然后將免疫細胞募集到腫瘤微環(huán)境(TME)中,通過皮下將具有或不具有circNDUFB2過表達的LLC1(LL / 2,鼠肺癌細胞系)細胞遞送至C57BL / 6小鼠 注射。 三周后,我們發(fā)現(xiàn)circNDUFB2過表達顯著抑制了體內(nèi)LLC1細胞的致瘤性,而在CircNDUFB2過表達LLC1細胞的小鼠中血清IFNβ的水平顯著升高。此外,在從這些小鼠解剖的腫瘤組織中檢測到CD8 + T細胞和DC的浸潤,并且circNDUFB2過表達顯著增加了TME中CD8 + T細胞和DC的頻率。最后,分析了52例NSCLC患者腫瘤組織中circNDUFB2與RIG-I或IFNβ之間的相關(guān)性。結(jié)果表明circNDUFB2與RIG-1和IFNβ正相關(guān)。 以上結(jié)果表明,RIG-1介導(dǎo)的circNDUFB2的免疫反應(yīng)抑制了腫瘤的進展。