小膠質細胞HO-1阻斷通過影響鐵死亡在衰老過程中發揮保護作用
研究背景:HO-1是一種抗炎、抗氧化和具有神經保護作用的誘導酶,但是,在衰老過程中和年齡相關疾病中,HO-1的表達增加與神經毒性鐵沉積有關。因為小膠質細胞與腦內固有免疫反應有關,Cristina Fern′ andez-Mendívil等人在Redox Biology(IF= 9.986)這一雜志上發表文章,闡明在炎癥條件下的老年鼠中小膠質細胞HO-1的作用。
技術路線圖:
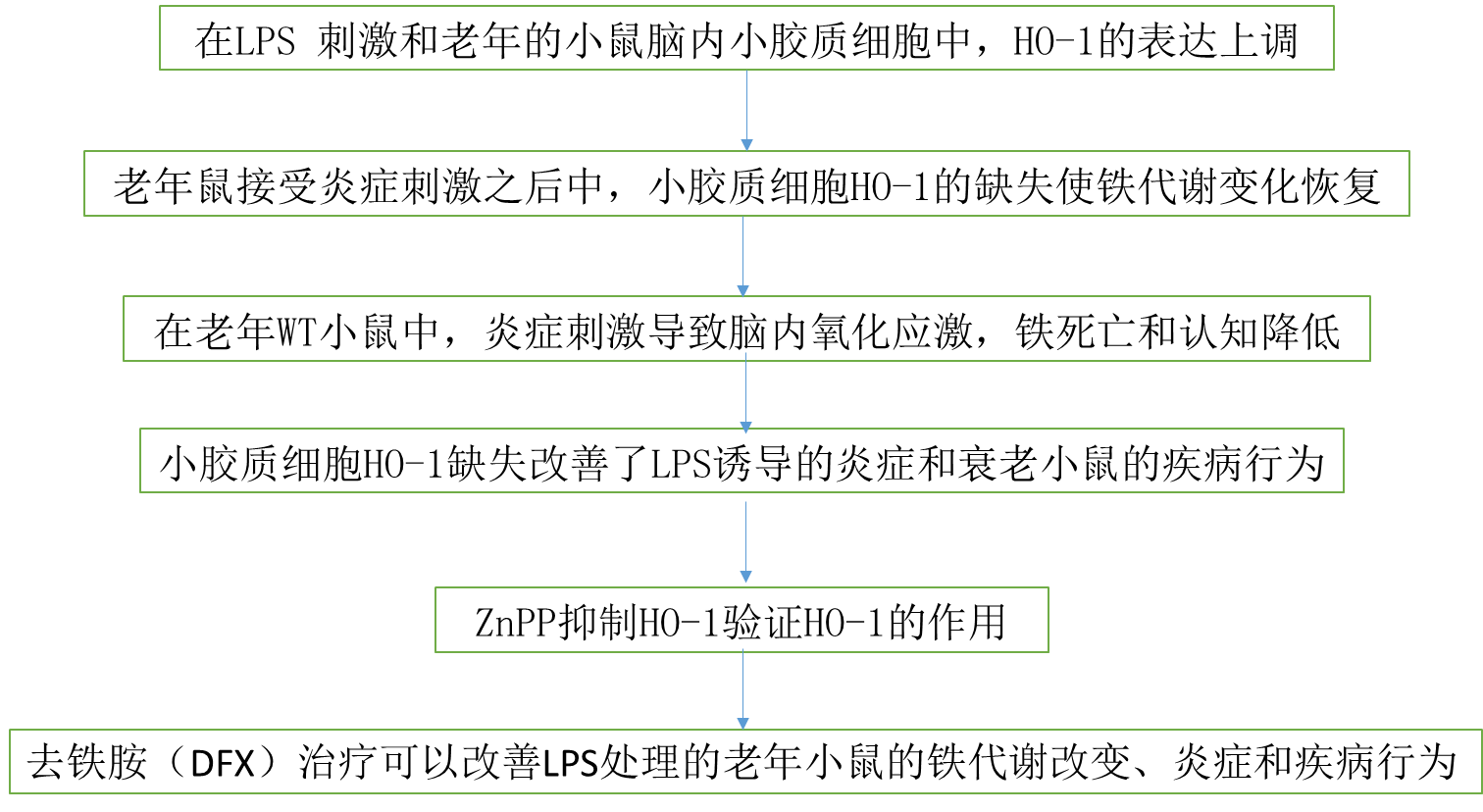
研究結果:
1. 在LPS 刺激和老年的小鼠腦內小膠質細胞中,HO-1的表達上調
與成年小鼠相比,老年小鼠的大腦中HO-1表達上調(圖1A-D)。圖1 A和E,與生理鹽水處理的老年鼠相比,LPS處理的老年鼠Iba1+小膠質細胞中HO-1水平顯著升高。結果表明,隨著年齡的增長,小膠質細胞HO-1表達上調,在急性炎癥損傷中,HO-1的過表達進一步增加。
Fig.1
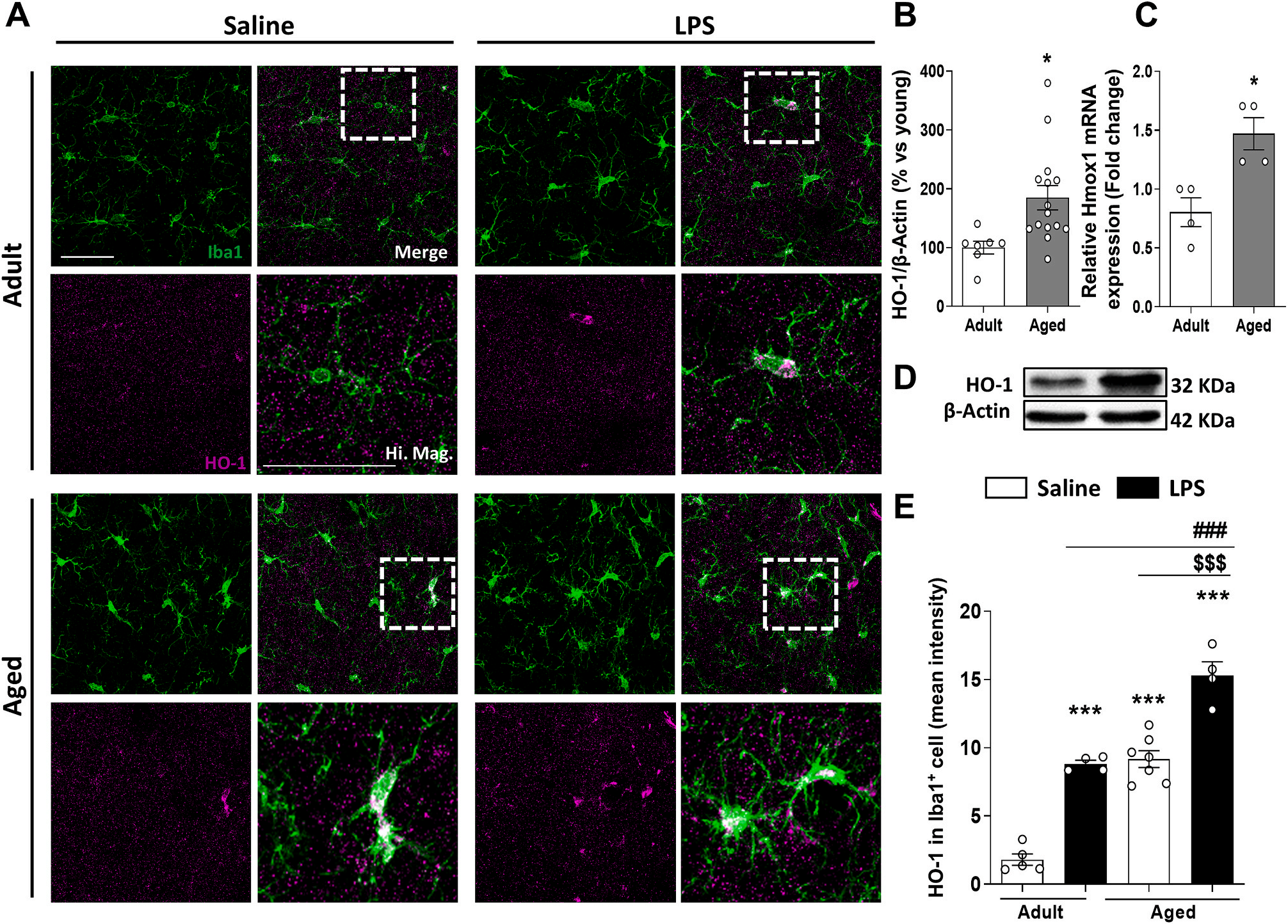
2. 老年鼠接受炎癥刺激之后,小膠質細胞HO-1的缺失使鐵代謝變化恢復
如圖2B所示,WT小鼠經lps注射之后腦內非血紅素鐵的含量顯著增加,但是在HMOX1M-KO小鼠中并沒有增加。此外,Perl s溶液染色顯示在注射LPS的WT小鼠海馬和皮質中鐵積累(圖2C和D),與生理鹽水WT小鼠相比。這些沉積在LPS刺激的HMOX1M-KO小鼠中較低(圖2C和D)。表明在衰老過程中LPS依賴的小膠質細胞HO-1上調可能在鐵沉積的形成中發揮關鍵作用。LPS處理的WT小鼠大腦中觀察到的鐵沉積與不同鐵代謝標志物的改變有關(圖2E)。鐵轉運體DMT1和鐵蛋白L-ferritin升高,而鐵轉運蛋白FPN1下降 (圖2E和F)。然而,這些改變在LPS處理的HMOX1M-KO小鼠中被逆轉,這意味著在衰老的WT小鼠中,LPS導致了鐵流入和儲存增多,而外排減少,從而導致鐵積累。在老化的HMOX1M-KO中,沒有鐵積累。
Fig.2
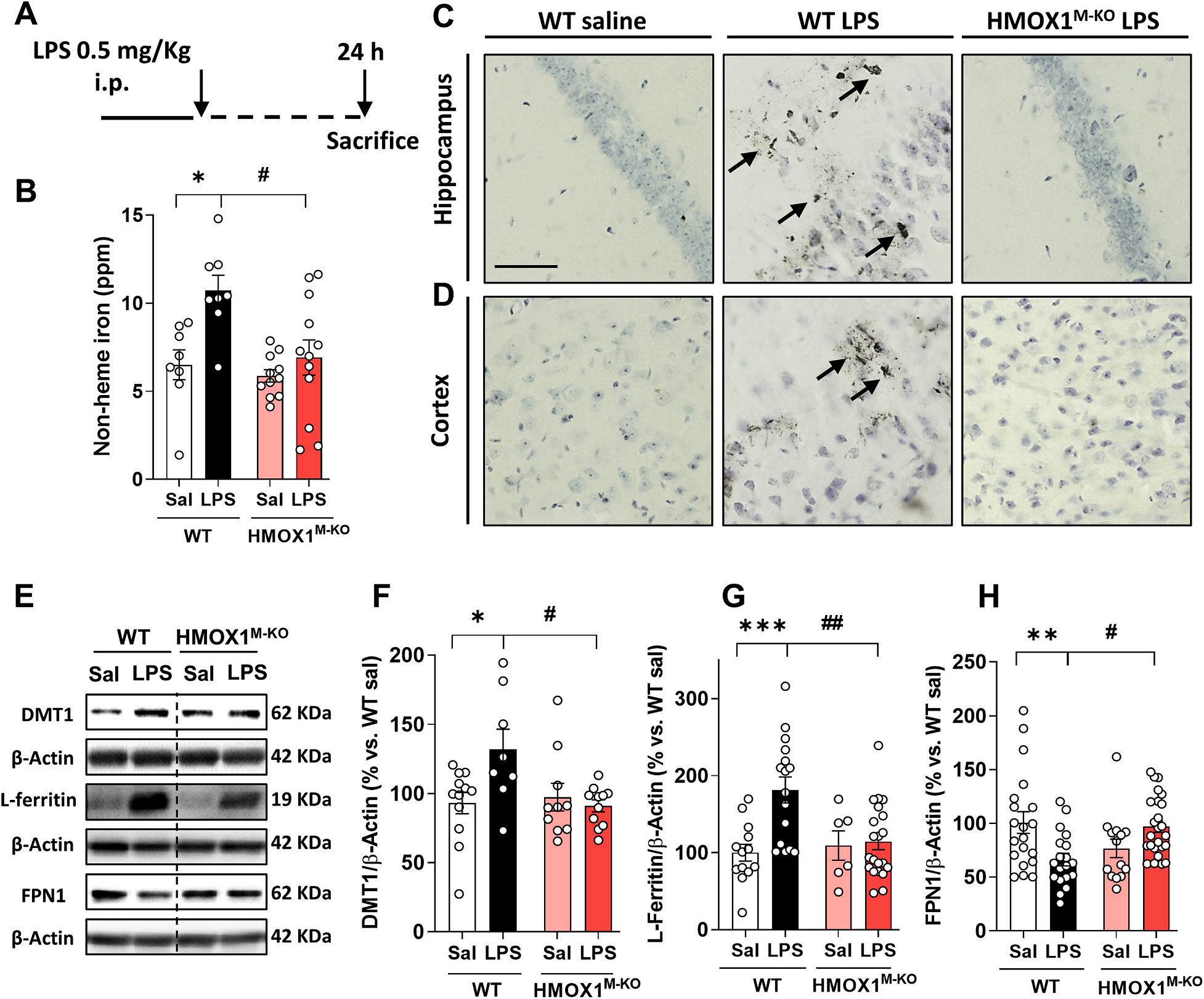
3. 在老年WT小鼠中,炎癥刺激導致腦內氧化應激,鐵死亡和認知降低
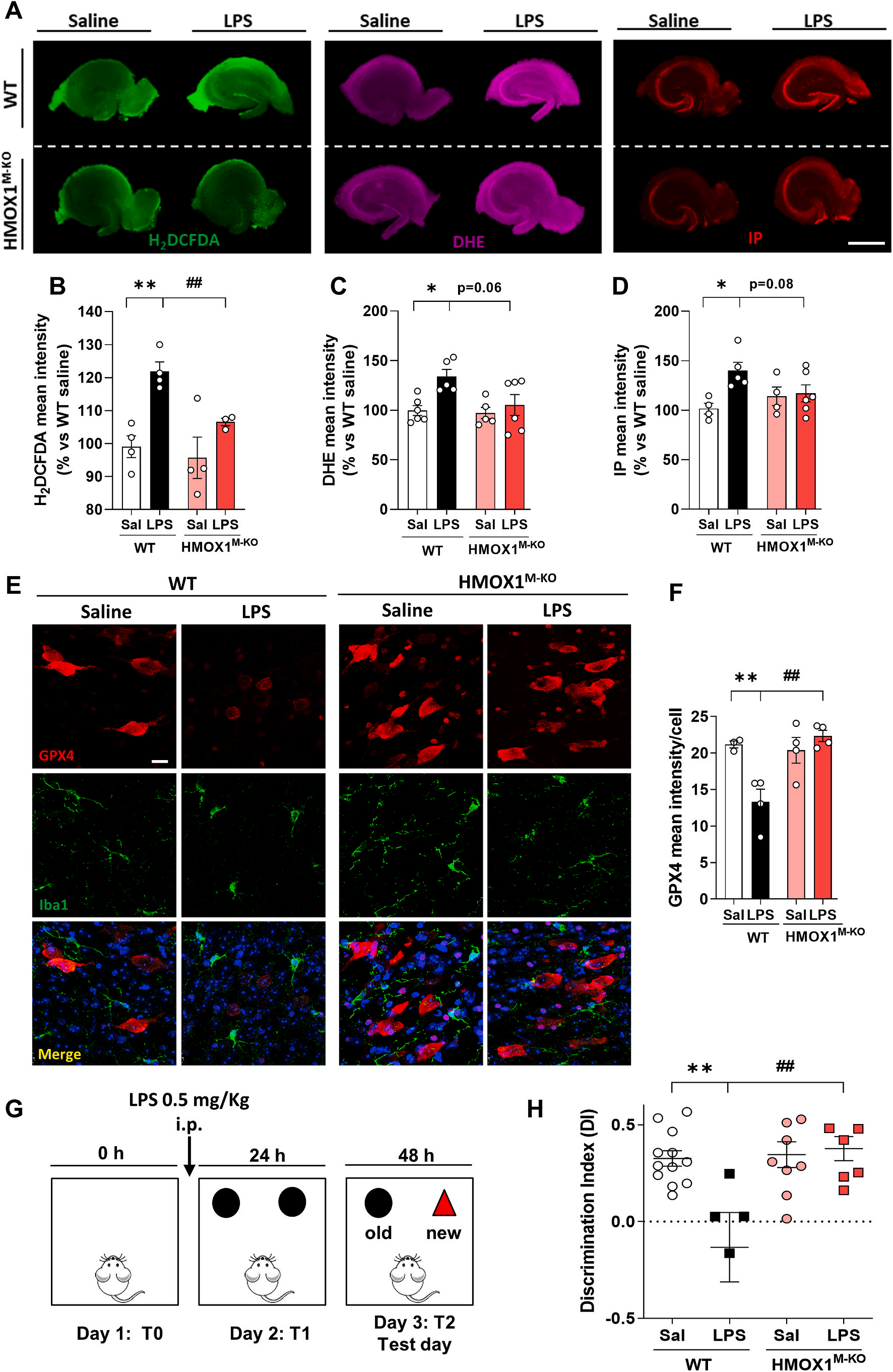
如圖3ABC, 熒光染料H2DCFDA和DHE標記小鼠海馬中ROS的產生,發現在老年WT小鼠中ROS顯著增加,而LPS刺激的HMOX1M-KO小鼠中,ROS減少。并且,通過圖3A和D 觀察PI染色發現,LPS注射WT小鼠會導致海馬細胞死亡的增加。LPS刺激的HMOX1M-KO小鼠中,細胞死亡減少。LPS注射WT小鼠GPX4的表達降低,HMOX1M-KO小鼠中沒有變化(圖3E和F)。由于鐵死亡導致神經元死亡,之后又研究LPS是否也會導致認知能力下降,通過NOR(新事物識別)任務進行評估 (圖3G)。事實上,LPS在WT小鼠中誘導了認知能力的下降,測量結果是DI的下降,但在HMOX1M-KO中沒有 (圖3H)。因此,這些結果表明,在年老的WT小鼠中觀察到LPS誘導的小膠質細胞HO-1的上調導致的的鐵積累,可能導致OS、鐵下垂,并最終導致認知能力下降。但是,LPS處理的HMOX1M-KO小鼠中,所有這些特征均顯著減弱并部分恢復。
Fig.3
4. 小膠質細胞HO-1缺失改善了LPS誘導的炎癥狀況和衰老小鼠的疾病行為
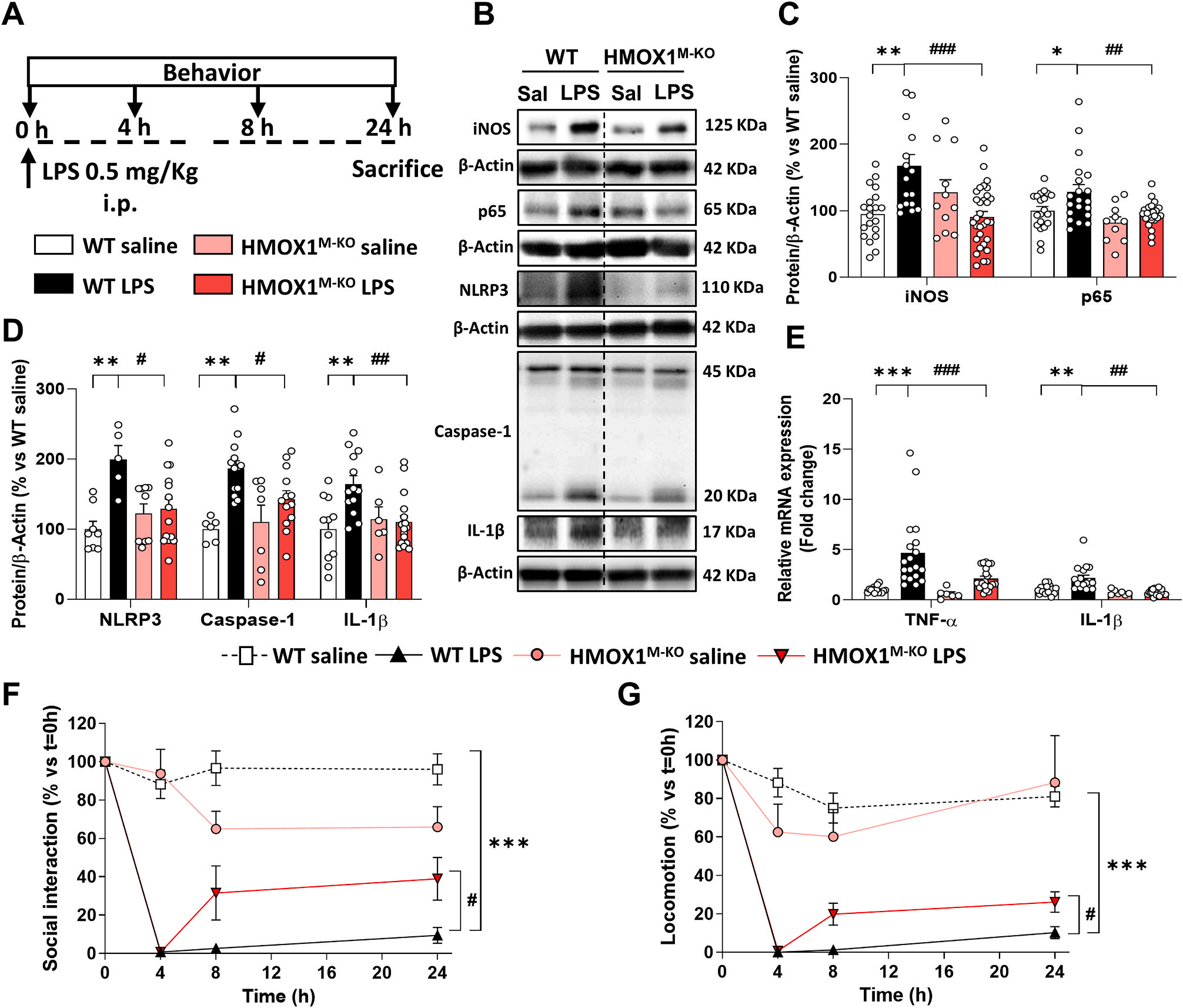
報道顯示鐵沉積與神經炎癥關系密切。之后,我們研究了LPS依賴性的小膠質細胞HO-1過表達,除了導致鐵代謝改變外,是否與腦內促炎改變相關,盡管其具有抗炎作用。我們分析了LPS注射24小時后海馬區不同的炎癥標志物(圖4A)。iNOS和p65,與炎癥小體相關蛋白質NLRP3、 caspase-1和IL- 1β,和細胞因子TNF -α和IL- 1β(圖4 e)。與注射鹽水的WT小鼠相比,注射LPS的WT小鼠中這些蛋白或細胞因子的表達顯著增加。然而,LPS刺激的HMOX1M-KO小鼠中這些參數顯著降低。
Fig.4
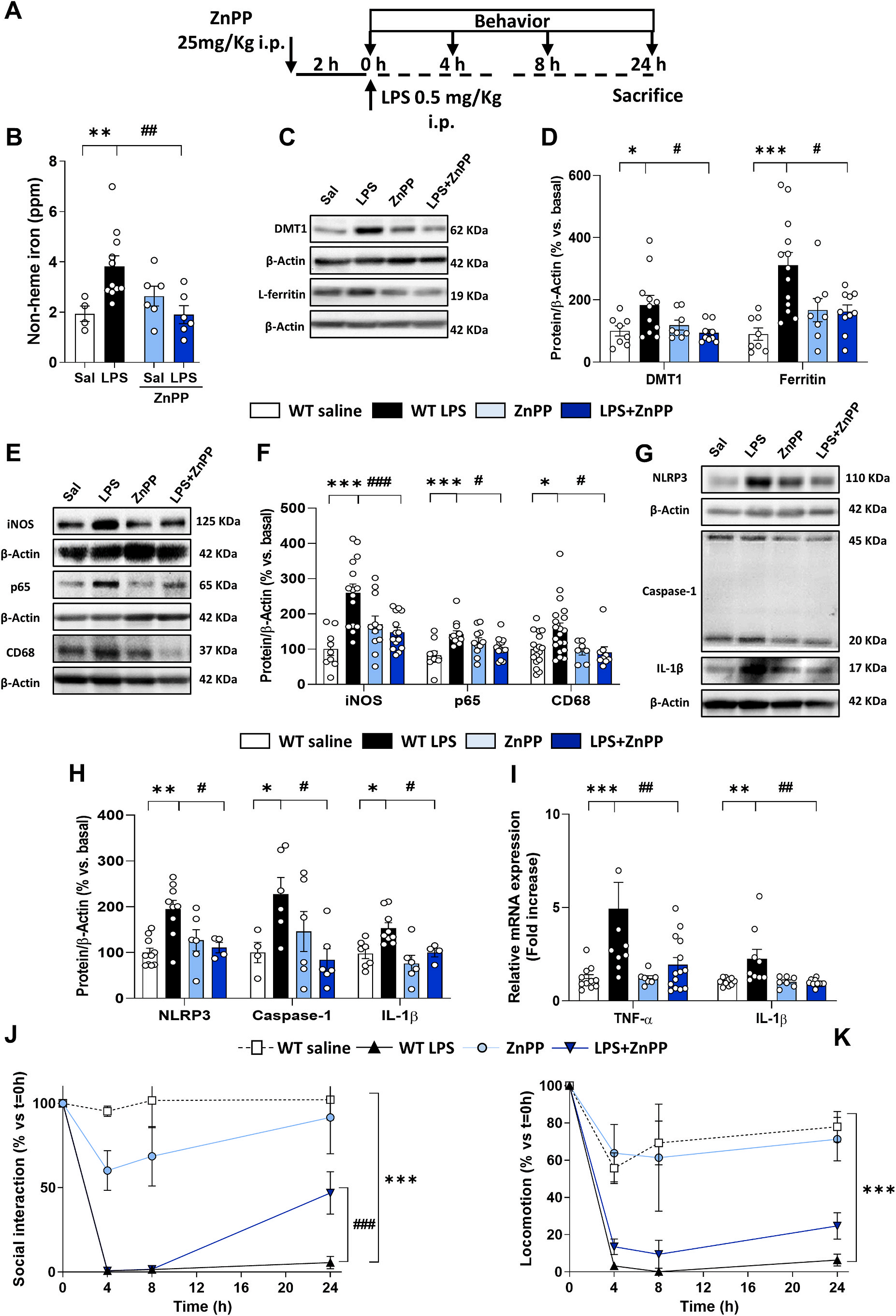
5. ZnPP對HO-1的藥理抑制可以恢復LPS引起的炎癥、氧化和鐵變化
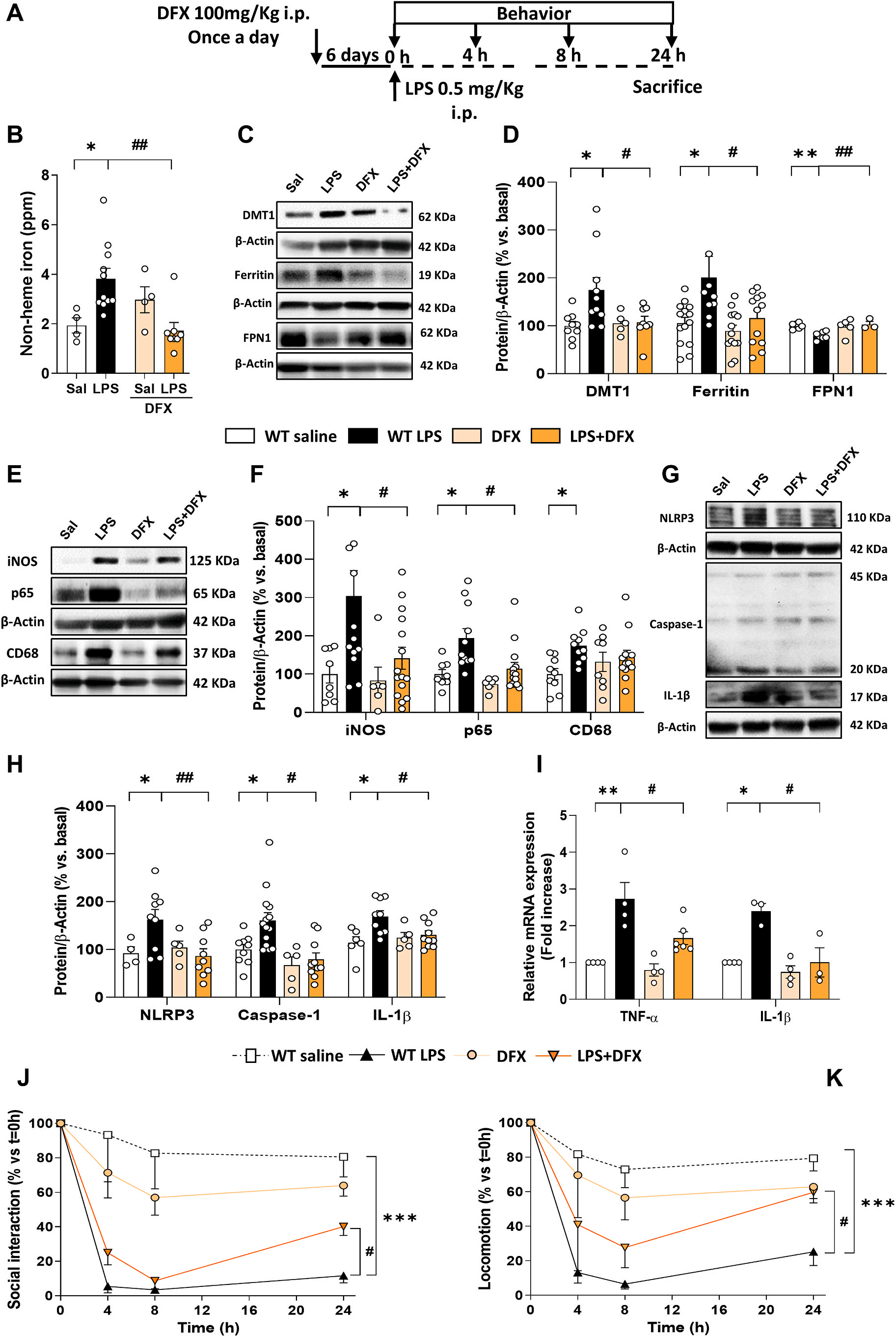
使用ZnPP作為HO-1抑制劑,證實遺傳小鼠模型獲得的結果。按照圖6A的方法。ZnPP減少了LPS誘導的非血紅素鐵的積累(圖6B), ZnPP能夠至少部分恢復LPS誘導的鐵代謝改變(圖6D)。此外,ZnPP處理降低了LPS誘導的iNOS、p65和CD68的增加(圖6E和F)、炎性體相關蛋白、IL-1β、NLRP3和caspase-1的表達(圖6G和H) 以及細胞因子TNF和IL-1表達減少(圖6I)。此外,ZnPP改善了小鼠在疾病行為測試中的表現(圖6J和K)。綜上所述,這些結果支持了HO-1在受到炎癥刺激的老年鼠中對鐵代謝、炎癥和行為改變的作用
Fig.5
6. 去鐵胺(DFX)治療可以改善LPS處理的老年小鼠的鐵代謝改變、炎癥和疾病行為
DFX能夠減少不穩定鐵(圖7B)并恢復LPS誘導的鐵代謝變化(圖7 c和D). 此外,DFX減少炎性標記物的表達,如iNOS和p65, 而不是CD68(圖7E和F)和炎性體相關標志物NLRP3、caspase-1和成熟IL-1 (圖7 g和H)。此外,DFX也減少了TNF-α和IL- 1β (圖7I)。此外,DFX改善了小鼠在疾病行為任務中的表現(圖7J和K)。DFX能夠恢復LPS處理的老年小鼠的大部分變化,這一事實表明,老年WT小鼠中,鐵負荷可能是LPS依賴性小膠質細胞HO-1過表達的結果,與炎癥、氧化應激和認知障礙有關。
Fig.6